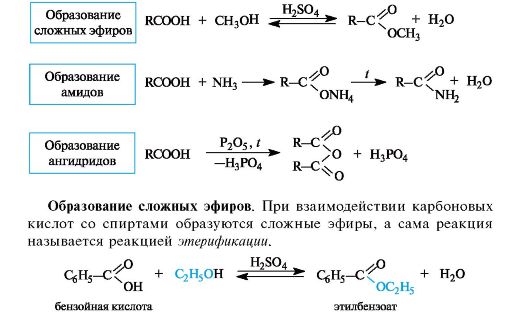
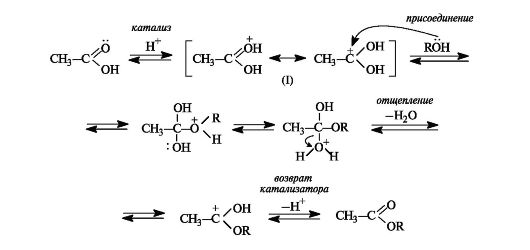
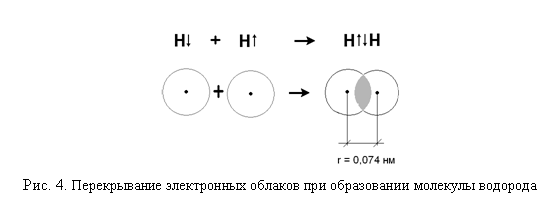
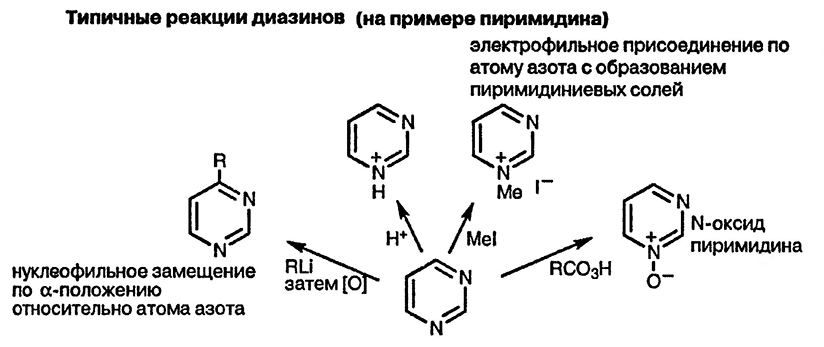
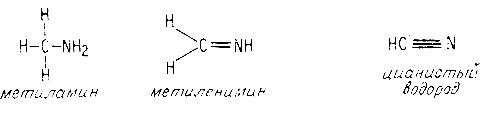Почему реакционная способность атома и молекулы азота различны
Вы точно человек?
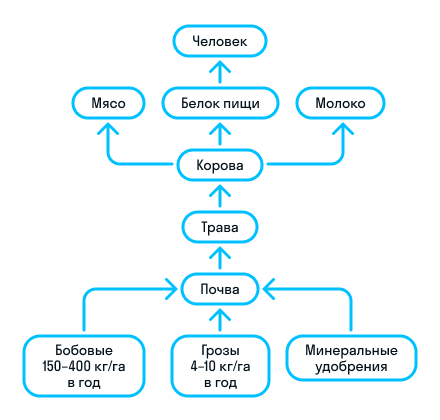
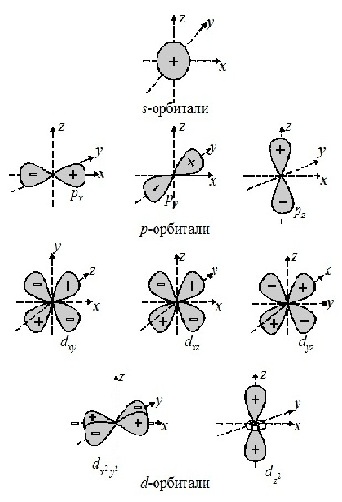
Атомы, образующие молекулы, всегда оказывают влияние друг на друга. Это влияние проявляется в молекулах с ковалентной полярной связью , то есть в соединениях, связь в которых образована за счёт общих электронных пар. Напомним, что ковалентная связь образуется между атомами неметаллов , при этом общая электронная пара всегда стянута к атому с большей электроотрицательностью. Например, в молекулах галогеноводородов общая электронная пара, образованная за счёт перекрывания электронных орбиталей водорода и галогена, стянута к атому галогена как более электроотрицательному элементу, а в молекуле аммиака — к атому азота. Это сказывается на свойствах вещества.


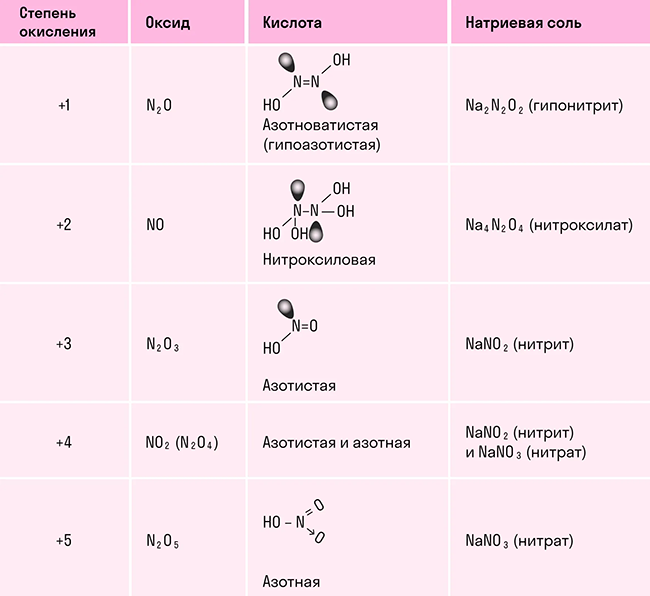
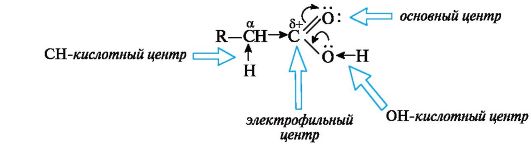



Общая характеристика химических элементов подгруппы азота. Подгруппа азота пниктогены — V группа, главная подгруппа «А» - азот, фосфор, мышьяк, сурьма, висмут. Свойства элементов V-A подгруппы.




Координационные и металлоорганические соединения, содержащие в своем составе редокс-активные лиганды, являются одной из перспективных точек развития современной химии и находят применение в целом ряде областей исследования, таких как фундаментальные вопросы теории химической связи, каталитические превращения органических субстратов и малых молекул, молекулярный магнетизм и многое другое [ 1 — 8 ]. Другим интенсивно развивающимся направлением координационной химии стали исследования соединений непереходных металлов в низких степенях окисления, обладающих уникальными химическими свойствами [ 9 — 13 ]. Среди них большое внимание уделяется двухвалентным производным элементов 14 группы — так называемым тяжелым аналогам карбенов. К настоящему времени в литературе накоплен большой массив информации о синтезе и химических свойствах стабильных гермиленов, станниленов и плюмбиленов [ 14 — 20 ].